
Для реакции ……………………………………………………………… определите возможное направление самопроизвольного течения реакции при стандартных условиях и при температуре t (Решение → 45589)
Заказ №78599
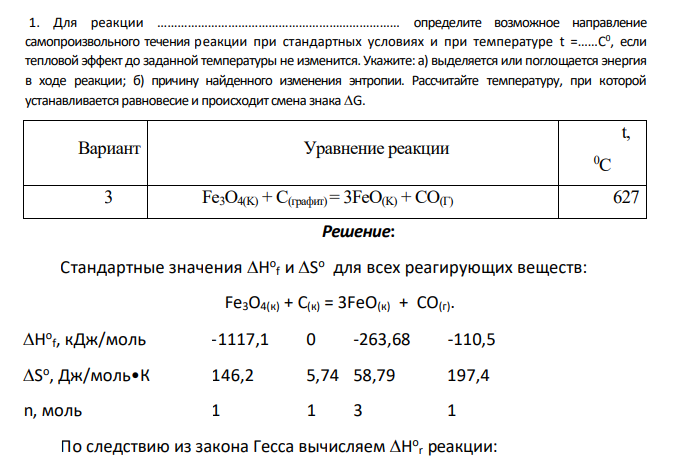
Для реакции ……………………………………………………………… определите возможное направление самопроизвольного течения реакции при стандартных условиях и при температуре t =……C 0 , если тепловой эффект до заданной температуры не изменится. Укажите: а) выделяется или поглощается энергия в ходе реакции; б) причину найденного изменения энтропии. Рассчитайте температуру, при которой устанавливается равновесие и происходит смена знака G. Вариант Уравнение реакции t, 0С 3 Fe3O4(K) + C(графит) = 3FeO(K) + CO(Г) 627
Решение:
Стандартные значения H o f и S o для всех реагирующих веществ: Fe3O4(к) + С(к) = 3FeО(к) + СО(г). H o f, кДж/моль -1117,1 0 -263,68 -110,5 S o , Дж/моль•К 146,2 5,74 58,79 197,4 n, моль 1 1 3 1 По следствию из закона Гесса вычисляем H o r реакции:

- К 0,8 л раствора гидроксида натрия с массовой долей 80,0 % и плотностью 1,328 г/мл прибавлено 0,4л раствора гидроксида натрия с массовой долей 14,0% и плотностью 1,153 г/мл
- В литре воды растворили 666,0 г гидроксида калия. Плотность полученного раствора 1,395 г/мл. Рассчитайте молярную концентрацию раствора
- Какой объем воды надо добавить к 100,0 мл 20,0%-го раствора серной кислоты плотностью 1,14 г/мл, чтобы получить 5,0%-й раствор
- В какой массе эфира надо растворить 3,04г анилина C6H5NH2, чтобы получить раствор с молярной концентрацией равной 0,3 моль/кг
- Какие объемы 2,0 М и 6,0 М растворов соляной кислоты надо смешать для приготовления 500,0 мл 3,0 М раствора? В ответе укажите объем 6,0 М раствора
- Три раствора одного и того же вещества, молярная концентрация которых 1,0 моль/л, 2,0 моль/л и 0,2 моль/л, смешали в объемных отношениях 1:2:7. Рассчитайте молярную концентрацию полученного раствора
- Сколько граммов кристаллогидрата хлорида кальция СаС12•6Н2О потребуются для приготовления 1750,0 г раствора с моляльной концентрацией 0,2 моль/кг
- На основании табличных значений G 0 обр реагентов определить возможность самопроизвольного протекания реакции при стандартных условиях
- Рассчитать количество выделенного тепла, если в процессе алюмотермии, описываемом уравнением 2 Al(к) + Fe2O3(к) = Al2O3(к) + 2Fe(к), прореагировало 2,7 кг алюминия
- Вычислить концентрацию С2О4 2- в 0,05М растворе щавелевой кислоты
- к 30мл 0,075М р-ра фосфорной кислоты добавили 15мл 0,15М рра едкого натра. Вычислить рН полученного раствора
- Почему металлические свойства элементов усиливаются в группах, но ослабевают в периодах Периодической системы? В чём отличие металлов от неметаллов
- Сформулируйте закон сохранения массы вещества, кем и когда он был открыт? Смешали растворы, содержащие 100 г гидроксида натрия и 200 г сульфата меди (II). Рассчитайте массу вещества, выпавшего в осадок
- Вычислите тепловой эффект реакции ……………………………………., пользуясь стандартными энтальпиями образования реагирующих веществ. Сколько теплоты выделится (поглотится) при образовании вещества
